PSE – Videokurs II
![]()
Chemie kann man üben!

![]()
![]()
► Warum sind manche Stoffe fest und andere gasförmig oder flüssig?
► Weshalb zeigen manche Stoffe ein Farbigkeit, während andere farblos erscheinen?
► Warum reagieren bestimmte Stoffe miteinander und andere kann man zusammen lagern, ohne dass Interaktionen geschehen?
► Wasser ist ein gutes Lösungsmittel, aber nicht für alle Stoffe. Wieso?
Die Antworten auf diese Fragen kann man mit chemischen Bindung erklären, die den beteiligten Teilchen zu Grunde liegt! Sie bestimmt die Neigung zur Zusammenlagerung oder Abstoßung. Damit also auch das chemische Verhalten gegen andere Stoffe, die stofflichen Zustände und auch die äußere Erscheinung der Stoffe.
Chemische Bindungen – also der Zusammenhalt der kleinsten Teilchen in Stoffen – beruhen auf der Annäherung von Atomen. Die dabei gewonnene Nähe führt zur unmittelbaren Anziehung von unterschiedlichen Ladungen. Kerne ziehen Elektronen anderer Atome ebenso an, wie ihre eigenen Elektronen. Die Außenelektronen fremder Atome sind dabei am meisten beeinflussbar.

Annäherung – Durchdringung – Elektronenpaarbindung (Atombindung)
Nach der Annäherung kommt es zur Durchdringung der Atomhüllen und damit zur Ausbildung von gemeinsamen Bereichen. Dort gibt es keine Zugehörigkeit von Elektronen zu ihrem Kern mehr.
Die Elektronen mit diesem Abstand vom fremden Kern – immer zwei – werden nun gemeinschaftlich genutzt. Es bilden sich gemeinsam genutzte „Elektronenpaare“ aus. Teilchen, die so verbunden sind haben eine Elektronenpaarbindung oder Atombindung. (Beispiele: Wasserstoff, Stickstoff, Sauerstoff, und weitere Nichtmetalle)

Die polare Atombindung/Elektronenpaarbindung)
Nähern sich zwei Partner mit unterschiedlichen Anziehungskräften (unterschiedliche Elektronegativität EN -Werte im PSE ), so entsteht eine polare Atombindung. Hier werden die Elektronen des „schwächeren Partners“(kleinerer EN Wert) stärker vereinnahmt und es entstehen Moleküle mit nach außen wirkenden Ladungsbereichen. Dies hat auf Löslichkeiten der Stoffe und ihre Neigung zur Zusammenlagerung von Teilchen also beispielsweise beim Aggregatzustand große Auswirkungen.

Die ionische Bindung – Ionenbeziehung
Bei zu hoher Anziehungskraft eines Partners – Elektronegativität – können die Außenelektronen auch vollständig in die Hülle des stärkeren Atoms wechseln. Es entsteht dann Ionen. Diese Bindungsart nennt man Ionenbeziehung.
Unterscheiden sich zwei Atomarten in ihrer Elektronegativität (EN) um mehr als 1,7 , so ist die Ionenbildung und damit die Ionenbindung sehr wahrscheinlich. Bei Natrium (EN= 0,9) und Chlor (EN=3,0) beträgt der Unterschied 2,1.
Wir kennen die Verbindung von Natrium und Chlor als Natriumchlorid, dem Kochsalz. Sie ist eine kristalline Ionensubstanz, die aus positiv und negativ geladenen Ionen besteht, wie alle Salze.

weiterführender Artikel:
► Weitere Bindungsanalysen
Arbeitsblätter zum Thema:
![]()
![]()

Betrachten wir die „andere“ Seite des PSE. Hier finden wir die Elemente „rechts“ der Bor-Astat-Linie.
Die Nichtmetalle sind Atomarten, die Elementsubstanzen aufbauen, die immer etwas „nicht metallisches“ an sich haben. So sind einige gasförmig bei Raumtemperatur oder sie leiten keinen elektrischen Strom, glänzen nicht oder sind schlechte Wärmeleiter. Irgendwas fehlt immer …
Einige Beispiele:
| Eigenschaften / Verwendungen | Kohlenstoff | Schwefel | Phosphor | Stickstoff |
|---|---|---|---|---|
| lateinischer Name/ Namensbedeutung | Carboneum / Holzkohle | Sulfur / langsam brennen, schwelen | Phosphorus /lichttragend, leuchtend | Nitrogenium/ salpeterbildend |
| Bau – Struktur der Modifikationen | Riesenmoleküle Graphit– geschichtet 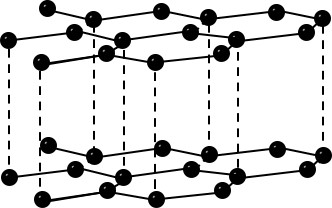 Diamant – Tetraedrisch dicht gepackter Kristall 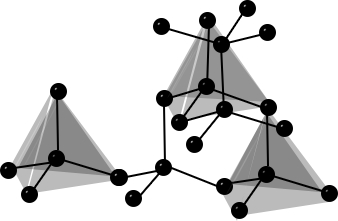 | 8-atomige räumlich orientierte Moleküle 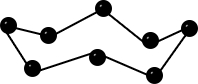 | Moleküle weiß – tetraedrisch 4-atomige Moleküle rot/schwarz – gewellte Doppelschichten 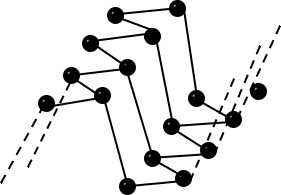 | 2-atomige Moleküle  |
| Dichte (g/cm³) | 2.267 | 2.07 | 1.82 | 1.251 |
| Schmelztemperatur (°C) | 3550 | 115 | 44.2 | -210.1 |
| Siedetemperatur (°C) | 4827 | 444.6 | 280 | -196 |
| Löslichkeit in Wasser | Unlöslich in Wasser | Unlöslich in Wasser, | Unlöslich in Wasser, | Unlöslich in Wasser, |
| Farbe | Schwarz, farblos | Gelb | Weiß, rot, schwarz | Farblos |
| Glanz | Diamant – lichtbrechend Graphit – grau glänzend | nein | nein | nein |
| Geruch | geruchlos | geruchlos | geruchlos | geruchlos |
| Brennbarkeit an der Luft | nicht brennbar | brennbar | brennbar | nicht brennbar |
| elektrische Leitfähigkeit | Graphit – ja Diamant – nein | nein | nein | nein |
| Verformbarkeit in der Kälte | nein | nein | nein | ja (gasförmig) |
| Verwendung | Schmuck (Diamant), Elektroden(Graphit), Kohlenstofffasern Bohr– und Schneidwerkzeuge (Diamant) | Schwefelsäure- und Düngemittelherstellung, | Düngemittel, Feuerwerkskörper, Flammenhemmer | Düngemittel, Kühlmittel, Ammoniakherstellung |
| natürliches Vorkommen | Diamanten- vulkanische Schlote und in Vergesellschaftung mit dem Mineral Kimberlit (Südafrika) | weltweit 1500 Fundorte (Polen, Sizilien,…) | weltweit in Form von Mineralien (Phosphate) | 78,1% der Luft |
Diese Atomarten bilden individuelle Elementsubstanzen von großer natürlicher, biologischer und technischer Bedeutung !
Beitrag: Kohlenstoff
Beitrag: Schwefel
Beitrag: Wasserstoff
Beitrag: Sauerstoff
Beitrag: Phosphor
![]()