Schwefel – Quiz
![]()
Chemie kann man üben!

![]()

Betrachten wir die „andere“ Seite des PSE. Hier finden wir die Elemente „rechts“ der Bor-Astat-Linie.
Die Nichtmetalle sind Atomarten, die Elementsubstanzen aufbauen, die immer etwas „nicht metallisches“ an sich haben. So sind einige gasförmig bei Raumtemperatur oder sie leiten keinen elektrischen Strom, glänzen nicht oder sind schlechte Wärmeleiter. Irgendwas fehlt immer …
Einige Beispiele:
| Eigenschaften / Verwendungen | Kohlenstoff | Schwefel | Phosphor | Stickstoff |
|---|---|---|---|---|
| lateinischer Name/ Namensbedeutung | Carboneum / Holzkohle | Sulfur / langsam brennen, schwelen | Phosphorus /lichttragend, leuchtend | Nitrogenium/ salpeterbildend |
| Bau – Struktur der Modifikationen | Riesenmoleküle Graphit– geschichtet 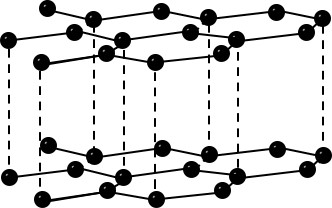 Diamant – Tetraedrisch dicht gepackter Kristall 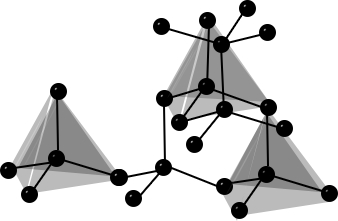 | 8-atomige räumlich orientierte Moleküle 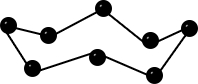 | Moleküle weiß – tetraedrisch 4-atomige Moleküle rot/schwarz – gewellte Doppelschichten 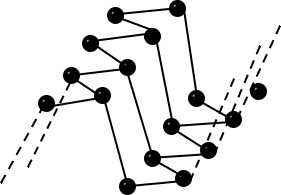 | 2-atomige Moleküle  |
| Dichte (g/cm³) | 2.267 | 2.07 | 1.82 | 1.251 |
| Schmelztemperatur (°C) | 3550 | 115 | 44.2 | -210.1 |
| Siedetemperatur (°C) | 4827 | 444.6 | 280 | -196 |
| Löslichkeit in Wasser | Unlöslich in Wasser | Unlöslich in Wasser, | Unlöslich in Wasser, | Unlöslich in Wasser, |
| Farbe | Schwarz, farblos | Gelb | Weiß, rot, schwarz | Farblos |
| Glanz | Diamant – lichtbrechend Graphit – grau glänzend | nein | nein | nein |
| Geruch | geruchlos | geruchlos | geruchlos | geruchlos |
| Brennbarkeit an der Luft | nicht brennbar | brennbar | brennbar | nicht brennbar |
| elektrische Leitfähigkeit | Graphit – ja Diamant – nein | nein | nein | nein |
| Verformbarkeit in der Kälte | nein | nein | nein | ja (gasförmig) |
| Verwendung | Schmuck (Diamant), Elektroden(Graphit), Kohlenstofffasern Bohr– und Schneidwerkzeuge (Diamant) | Schwefelsäure- und Düngemittelherstellung, | Düngemittel, Feuerwerkskörper, Flammenhemmer | Düngemittel, Kühlmittel, Ammoniakherstellung |
| natürliches Vorkommen | Diamanten- vulkanische Schlote und in Vergesellschaftung mit dem Mineral Kimberlit (Südafrika) | weltweit 1500 Fundorte (Polen, Sizilien,…) | weltweit in Form von Mineralien (Phosphate) | 78,1% der Luft |
Diese Atomarten bilden individuelle Elementsubstanzen von großer natürlicher, biologischer und technischer Bedeutung !
Beitrag: Kohlenstoff
Beitrag: Schwefel
Beitrag: Wasserstoff
Beitrag: Sauerstoff
Beitrag: Phosphor
![]()
Material: Arbeitsblatt Schwefel

Element Nummer 16 wird „Sulfur“ – abgeleitet von „langsam brennen“ – genannt und ist dem Menschen schon seit dem Altertum bekannt. Schwefel wird schon 5000 v. Chr. erwähnt, da es als Arzneimittel (Augen), zum Bleichen von Textilien und zur Desinfektion genutzt wurde. Man findet Schwefel noch heute an der Erdoberfläche an den Austrittsöffnungen von Vulkanen und in ehemaligen vulkanischen Gebieten. Über besonders große Vorkommen verfügen Russland, Polen, Sizilien, USA, Kanada, u.a.
Zur Gewinnung aus dem Erdinneren wurde bis in das Jahr 2000 das Frasch Verfahren genutzt, bei dem mit einem doppelwandigen Rohr 155°C heißes Wasser in die Erde gepumpt wurde und der dadurch gelöste Schwefel (Schmelztemperatur 119,6°C) im Inneren des Rohres nach oben gesaugt werden konnte. Heute wird Schwefel als Nebenprodukt aus Erdgas/Erdöl im Claus Prozess gewonnen und fällt dort so reichlich an, dass eine unterirdische Produktion unrentabel ist.
[smartslider3 slider=“10″]
Was macht den Schwefel zum typischen Nichtmetall?
Schwefel ist spröde und leitet keinen Strom. Außerdem fehlt dem Element der typisch metallische Glanz.
Was weiß der Chemiker über Schwefel und wozu wird Schwefel eigentlich benötigt?
[smartslider3 slider=“11″]
Verbrennt man den Schwefel , so entsteht ein Gas mit dem typisch stechenden Geruch, Schwefeldioxid.
Dieses Gas löst sich gut in Wasser. Dabei kommt es zu einer chemischen Reaktion.
\( SO_2 + H_2O \longrightarrow H_2SO_3 \)
Brennender Schwefel an einem Vulkan in Indonesien
![]()